Savdo belgisi: Semavic®
Xalqaro patentlanmangan nomi (XPN): semaglutid
Dori shakli: teri ostiga yuborish uchun eritma
Tarkibi: 1 mL eritma quyidagilarni o’z ichiga oladi: ta’sir etuvchi modda: semaglutid – 1,34 mg; yordamchi moddalar: disodyum hidrofosfat dihidrat – 1,42 mg, propilen glikol – 14,0 mg, fenol – 5,5 mg, suyultirilgan vodorod xlorid kislotasi 10 % va/yoki natriy gidroksid eritmasi 10 % – pH ni 7,4 gacha tuzatish uchun, suvva inyektsiya uchun – 1 mL gacha.
Ta’rif: shaffof rangsiz yoki deyarli rangsiz eritma.
Dori vositasining farmakoterapevtik guruhi: gipoglikemik vosita glyukagonsifat peptid-1 (GSP1) muqobilidir.
ATK kodi: А10В106.
Farmokologik xususiyatlar
Semaglutid kimyoviy sintez orqali ishlab chiqarilgan GSP-1 retseptorlari (GSP-1R) agonistidir. Semaglutid 94 % inson GSP-1ga o’xshash GSP-1 muqobilidir. Semaglutid GSP-1R ni tanlab bog’laydigan va faollashtiradigan GSP-1R agonisti sifatida ishlaydi. GSP-1R mahalliy GSP-1 uchun maqsad bo’lib xizmat qiladi. GSP-1 fiziologik gormon bo’lib, glyukoza kontsentratsiyasini va ishtahani tartibga solishga, shuningdek, yurak-qon tomir tizimiga (YQT) bir nechta ta’sir ko’rsatadi. Glyukoza kontsentratsiyasi va ishtahaga ta’siri, ayniqsa, oshqozon osti bezi va miyada joylashgan GSP-1R tomonidan amalga oshiriladi. Semaglutidning farmakologik kontsentratsiyasi quyida tavsiflangan ta’sirlarning kombinatsiyasi orqali qondagi glyukoza kontsentratsiyasini va tana vaznini kamaytiradi. GSP-1R shuningdek, yurak, qon tomirlari, immunitet tizimi va buyraklarning muayyan hududlarida mavjud bo’lib, ularning faollashishi yurak-qon tomir (YQ) va mikrosirkulyatsiya ta’siriga ega bo’lishi mumkin. Mahalliy GSP-1 dan farqli o’laroq, semaglutidning yarimparchalanish davri (taxminan 1 hafta) uni haftada bir marta teri ostiga (SC) yuborish imkonini beradi. Albumin bilan bog’lanish semaglutidning uzoq muddatli ta’sirining asosiy mexanizmi bo’lib, buyraklar orqali chiqarilishini kamaytiradi va metabolik buzilishdan himoya qiladi. Bundan tashqari, semaglutid dipeptidil peptidaza-4 fermenti tomonidan degradatsiyaga qarshi barqarordir. Semaglutid insulin sekretsiyasini glyukozaga bog’liq faollashtirish va glyukagon sekretsiyasini bostirish orqali qondagi glyukoza kontsentratsiyasini pasaytiradi. Shunday qilib, qonda glyukoza kontsentratsiyasining oshishi bilan insulin sekretsiyasi faollashtiriladi va glyukagon sekretsiyasi bostiriladi. Glyukemik darajasini pasaytirish mexanizmi, shuningdek, erta postprandial (ovqatdan keyingi) fazada oshqozonni bo’shatishning biroz kechikishini ham o’z ichiga oladi. Gipoglikemiya davrida semaglutid insulin sekretsiyasini kamaytiradi va glyukagon sekretsiyasini kamaytirmaydi. Semaglutid energiya iste’molini kamaytirish orqali umumiy tana vaznini va yog’ to’qimalarining massasini kamaytiradi. Bu mexanizm ishtahaning umumiy pasayishini o’z ichiga oladi, shu jumladan to’yinganlik signallarining ortishi va ochlik signallarining kamayishi, shuningdek, oziq-ovqat iste’molini nazorat qilishni yaxshilash va oziq-ovqatga bo’lgan ishtahani kamaytirish. Insulin qarshiligi ham kamayadi, ehtimol tana vaznining pasayishi tufayli. Bundan tashqari, semaglutid yuqori yog’li ovqatlar uchun afzallikni kamaytiradi. Hayvonlarni o’rganish shuni ko’rsatdiki, semaglutid miyaning muayyan hududlari tomonidan qabul qilinadi va asosiy to’yinganlik signallarini oshiradi va asosiy ochlik signallarini susaytiradi. Miya to’qimalarining ajratilgan joylariga ta’sir qilib, semaglutid to’yinganlik hissi bilan bog’liq neyronlarni faollashtiradi va ochlik hissi bilan bog’liq neyronlarni bostiradi. Klinik tadqiqotlarda (KT) semaglutid plazma lipidlariga ijobiy ta’sir ko’rsatdi, sistolik qon bosimini (QB) pasaytirdi va yallig’lanishni kamaytiradi. Hayvonlarni o’rganishda semaglutid aterosklerozning rivojlanishini bostiradi, aorta plaklarining keyingi rivojlanishiga to’sqinlik qiladi va blyashkalarda yallig’lanishni kamaytiradi.
Farmakologik dinamikasi
Barcha farmakodinamik tadqiqotlar 12 haftalik terapiyadan so’ng (dozani oshirish davrini o’z ichiga olgan holda) haftada bir marta 1 mg semaglutidning barqaror konsentratsiyasida o’tkazildi.
Och qoringa va ovqatdan keyin qondagi glyukoza darajasi
Semaglutid ochlikdagi glyukoza kontsentratsiyasini va ovqatdan keyin glyukoza kontsentratsiyasini kamaytiradi. Platsebo bilan solishtirganda, 2-toifa qandli diabet (QD2) bo’lgan bemorlarda 1 mg semaglutid bilan davolash glyukoza kontsentratsiyasining mutlaq o’zgarishi (mmol/L) bo’yicha glyukoza kontsentratsiyasining pasayishiga va platsebo (%) bilan solishtirganda nisbiy kamayishiga olib keldi: ochlik glyukoza konsentratsiyasi (1,6 mmol/L; 22 %); glyukoza konsentratsiyasi ovqatdan keyin 2 soat o’tgach (4,1 mmol/L; 37 %); o’rtacha kunlik glyukoza kontsentratsiyasi (1,7 mmol/L; 22 %) va 3 ta ovqat uchun ovqatdan keyin eng yuqori glyukoza konsentratsiyasi (0,6-1,1 mmol/L). Semaglutid birinchi dozadan keyin ochlikdagi glyukoza kontsentratsiyasini kamaytiradi.
Pankreatik beta hujayralari funktsiyasi va insulin sekretsiyasi
Semaglutid ochlikdagi glyukoza kontsentratsiyasini va ovqatdan keyin glyukoza kontsentratsiyasini kamaytiradi. Platsebo bilan solishtirganda, 2-toifa qandli diabet (QD2) bo’lgan bemorlarda 1 mg semaglutid bilan davolash glyukoza kontsentratsiyasining mutlaq o’zgarishi (mmol/L) bo’yicha glyukoza kontsentratsiyasining pasayishiga va platsebo (%) bilan solishtirganda nisbiy kamayishiga olib keldi: ochlik glyukoza konsentratsiyasi (1,6 mmol/L; 22 %); glyukoza konsentratsiyasi ovqatdan keyin 2 soat o’tgach (4,1 mmol/L; 37 %); o’rtacha kunlik glyukoza kontsentratsiyasi (1,7 mmol/L; 22 %) va 3 ta ovqat uchun ovqatdan keyin eng yuqori glyukoza konsentratsiyasi (0,6-1,1 mmol/L). Semaglutid birinchi dozadan keyin ochlikdagi glyukoza kontsentratsiyasini kamaytiradi.
Glyukagon sekretsiyasi
Semaglutid ochlikdagi glyukagon kontsentratsiyasini va ovqatdan keyin glyukagon kontsentratsiyasini kamaytiradi. QD2 bilan og’rigan bemorlarda semaglutid platsebo bilan solishtirganda glyukagon kontsentratsiyasining nisbiy pasayishiga olib keladi: ochlikdagi glyukagon kontsentratsiyasi (8–21 %), ovqatdan keyin glyukagonning javobi (14–15 %) va o’rtacha kunlik glyukagon kontsentratsiyasi (12 %).
Insulinning glyukozaga qaram sekretsiyasi va glyukozaga bog’liq glyukagon sekretsiyasi
Semaglutid insulin sekretsiyasini rag’batlantirish va glyukozaga bog’liq holda glyukagon sekretsiyasini kamaytirish orqali yuqori qon glyukoza kontsentratsiyasini pasaytirdi. QD2 bilan og’rigan bemorlarga semaglutid kiritilgandan keyin insulin sekretsiyasi darajasi sog’lom ko’ngillilar bilan taqqoslangan. Induktsiyalangan gipoglikemiya davrida semaglutid platsebo bilan solishtirganda glyukagon kontsentratsiyasining ortishiga qarshi regulyatsiya reaktsiyasini o’zgartirmadi va QD2 bilan og’rigan bemorlarda C-peptid kontsentratsiyasining pasayishini kuchaytirmadi.
Oshqozonni bo’shatish
Semaglutid ovqatdan keyin oshqozonning erta bo’shatilishini biroz kechiktirdi va shu bilan ovqatdan keyin glyukozaning qonga kirish tezligini pasaytirdi.
Tana vazni va tana tuzilishi
Semaglutid bilan tana vaznining o’rganilgan taqqoslashlar (platsebo, sitagliptin, sekin tarzda chiqariladigan eksenatid (SCh), dulaglutid va insulin glargin) bilan solishtirganda ko’proq kamayishi kuzatildi. (“Klinik samaradorlik va xavfsizlik” bo’limiga qarang). Semaglutid bilan vazn yo’qotish, birinchi navbatda, yog’ to’qimalarining yo’qolishi bilan bog’liq bo’lib, bu mushak massasining yo’qolishidan 3 barobar ko’p edi.
Ishtaha, kaloriya iste’moli va oziq-ovqat tanlovi
Platsebo bilan solishtirganda, semaglutid ad libltum ketma-ket uchta ovqat paytida kaloriya iste’molini 18–35 % ga kamaytirdi. Bunga och qoringa ham, ovqatdan keyin ham semaglutid tomonidan qo’zg’atilgan ishtahani bostirish, oziq-ovqat iste’molini nazorat qilishni yaxshilash va oziq-ovqatga, ayniqsa yog’li ovqatlarga bo’lgan ishtiyoqni kamaytirishga yordam berdi.
Och qorin va ovqatdan keyin lipidlar
Platsebo bilan solishtirganda, semaglutid ochlik triglitseridlari va juda past zichlikdagi lipoproteinlar (JPZLP) xolesterin kontsentratsiyasini mos ravishda 12% va 21% ga kamaytirdi. Ko’p yog’li ovqatga javoban triglitseridlar va kichik zichlikdagi lipoproteinlar (KZLP) xolesterin konsentratsiyasining ovqatdan so’ng o’sishi 40 % dan ko’proq kamaydi.
Yurak elektrofiziologiyasi (YuEF)
Semaglutidning yurakdagi repolarizatsiya jarayoniga ta’siri YuEF tadqiqotida sinovdan o’tkazildi. Semaglutidni terapevtik dozalardan oshib ketadigan dozalarda qo’llash (1,5 mg gacha bo’lgan muvozanat konsentratsiyasida) tuzatilgan QT oralig’ining uzayishiga olib kelmadi.
Farmokologik kinetika
Dori vositasi haftada bir marta qo’llanilishi mumkin, chunki semaglutidning yarimparchalanish davri taxminan 1 hafta.
Singdirilishi
Plazmadagi maksimal kontsentratsiyaga (Cmax) erishish vaqti dozadan keyin 1 kundan 3 kungacha bo’lgan. dori vositasining muvozanat konsentratsiyasiga (AUCt/24) dori vositasini bir martalik haftalik foydalanishdan 4-5 hafta o‘tgach erishildi. Semaglutidni 0,5 mg va 1 mg dozada teri ostiga yuborishdan so’ng, QD2 bilan og’rigan bemorlarda uning o’rtacha muvozanat konsentratsiyasi mos ravishda taxminan 16 nmol/L va 30 nmol/L ni tashkil etdi. Semaglutidning 0,5 mg va 1 mg dozalariga ta’sir qilish yuborilgan dozaga mutanosib ravishda ortadi. Semaglutidni qorin old devoriga, son yoki elkaga teri ostiga yuborish bilan xuddi shunday ta’sirga erishiladi. Semaglutidning mutlaq bioavailability teri ostiga yuborilganidan keyin 89% ni tashkil etdi.
Taqsimlash
QD2 bilan og’rigan bemorlarga teri ostiga yuborilganidan keyin semaglutidning to’qimalarda o’rtacha tarqalish hajmi taxminan 12,5 litrni tashkil etdi. Semaglutid plazma albumini bilan sezilarli darajada bog’langan (>99 %).
Biotransformatsiya
Semaglutid oqsil peptid magistralining proteolitik bo’linishi va yon zanjirning yog’ kislotasining keyingi beta-oksidlanishi orqali metabollanadi.
Yo’q qilish
Oshqozon-ichak trakti (OIT) va buyraklar semaglutid va uning metabolitlarini yo’q qilishning asosiy yo’llari hisoblanadi. Semaglutidning yuborilgan dozasining 2/3 qismi buyraklar orqali, 1/3 qismi esa ichak orqali chiqariladi. Qabul qilingan dozaning taxminan 3 % buyraklar tomonidan o’zgarmagan semaglutid shaklida chiqariladi. QD2 bilan og’rigan bemorlarda semaglutidning klirensi taxminan soatiga 0,05 L/ni tashkil etdi. Taxminan 1 haftalik yarimparchalanish davri bilan semaglutid dori vositasining oxirgi dozasidan keyin taxminan 5 hafta davomida umumiy qon aylanishida mavjud bo’ladi.
Bemor maxsus guruhlari
Semaglutidning dozasini yoshga, jinsga, irqiy va millatga, tana vazniga yoki buyrak yoki jigar etishmovchiligining mavjudligiga qarab sozlash talab qilinmaydi.
Yoshi
20 yoshdan 86 yoshgacha bo’lgan bemorlarni o’z ichiga olgan 3-bosqich tadqiqoti davomida olingan ma’lumotlarga asoslanib, yosh semaglutidning farmakokinetikasiga ta’sir qilmagani ko’rsatilgan.
Jinsi
Jins semaglutidning farmakokinetikasiga ta’sir qilmadi.
Irqi
Irqiy guruh (oq, qora yoki afro-amerikalik, osiyolik) semaglutidning farmakokinetikasiga ta’sir qilmadi.
Etnik kelib chiqishi
Etnik kelib chiqishi (lotin amerkalik) semaglutidning farmakokinetikasiga ta’sir qilmadi.
Tana massasi
Tana vazni semaglutid ta’siriga ta’sir qildi. Yuqori tana og’irligi ta’sir qilishning pastligiga olib keladi. Semaglutidning 0,5 mg va 1 mg ga teng dozalari 40 dan 198 kg gacha bo’lgan tana vaznida dori vositasining yetarli darajada ta’sirini ta’minlaydi.
Buyrak yetishmovchiligi
Buyrak yetishmovchiligi semaglutidning farmakokinetikasiga klinik jihatdan ahamiyatli ta’sir ko’rsatmadi. Bu 0,5 mg semaglutidning bir martalik dozasini o’rganishda buyrak funktsiyasi normal bo’lgan bemorlarga nisbatan turli darajadagi buyrak yetishmovchiligi bo’lgan bemorlarda (yengil, o’rtacha, og’ir yoki dializ bilan og’rigan bemorlarda) ko’rsatilgan. Bu, shuningdek, QD2 va buyrak yetishmovchiligi bo’lgan bemorlarda KI 3a faza ma’lumotlari asosida ko’rsatilgan, ammo buyrak yetishmovchiligining oxirgi bosqichi bo’lgan bemorlarda tajriba cheklangan.
Jigar yetishmovchiligi
Jigar yetishmovchiligi semaglutid namoyon bo’lishiga ta’sir qilmadi. Semaglutidning farmakokinetik xususiyatlari jigar funktsiyasi normal bo’lgan bemorlarga nisbatan turli darajadagi jigar yetishmovchiligi (engil, o’rtacha, og’ir) bo’lgan bemorlarda 0,5 mg ga teng semaglutidning bitta dozasini o’rganishda baholandi.
Bolalar va o’smirlar
Semaglutid 18 yoshgacha bo'lgan bolalar va o'smirlarda o'rganilmagan.
Foydalanish uchun ko’rsatmalar
Semavic® 2-toifa qandli diabet bilan og’rigan kattalardagi bemorlarda glyukemik nazoratni yaxshilash uchun parhez va jismoniy mashqlar bilan birga foydalanish uchun ko’rsatiladi:
Semavic® yurak-qon tomir kasalliklarini standart davolashga qo’shimcha sifatida 2-toifa qandli diabet va yuqori yurak-qon tomir kasalliklari bilan og’rigan bemorlarda asosiy yurak-qon tomir kasalliklari * xavfini kamaytirish uchun tavsiya etiladi (birinchi yirik yurak-qon tomir hodisasining paydo bo’lish vaqtini tahlil qilish asosida – “Farmakologik xususiyatlar” bo’limiga qarang, “Yurak-qon tomir (Kardiovaskulyar) hodisalarning ta’siri” bo’limiga qarang).
*asosiy yurak-qon tomir hodisalariga quyidagilar kiradi: yurak-qon tomir kasalliklari tufayli o’lim, o’limga olib kelmaydigan miyokard infarkti, o’limga olib kelmaydigan insult.
Qo’llash mumkin bo’lmagan holatlar
Samaradorlik va xavfsizlik to’g’risida ma’lumotlar yo’qligi yoki foydalanish bo’yicha cheklangan tajriba tufayli quyidagi bemorlar/kasalliklarda Semavic® dan foydalanishga qarshi ko’rsatilgan:
Ehtiyotkorlik bilan
Semavic® dori vositasini buyrak yetishmovchiligi bo’lgan bemorlarda va pankreatit tarixi bo’lgan bemorlarda ehtiyotkorlik bilan qo’llash tavsiya etiladi (“Maxsus ko’rsatmalar” bo’limiga qarang).
Homiladorlik va emizish davrida foydalaning
Homiladorlik
Hayvonlarda o’tkazilgan tadqiqotlar dori vositasining reproduktiv toksikligini ko’rsatdi (“Klinikgacha bo’lgan xavfsizlik ma’lumotlari” bo’limiga qarang). Homilador ayollarda semaglutiddan foydalanish bo’yicha ma’lumotlar cheklangan. Homiladorlik davrida semaglutiddan foydalanish ta’qiqlangan. Reproduktiv salohiyati saqlanib qolgan ayollarga semaglutid bilan davolash paytida kontratseptsiya vositalaridan foydalanish tavsiya etiladi. Agar bemor homiladorlikka tayyorgarlik ko’rayotgan bo’lsa yoki homiladorlik allaqachon sodir bo’lgan bo’lsa, semaglutid terapiyasini to’xtatish kerak. Yarimparchalanish davri uzoq bo’lganligi sababli, semaglutid bilan davolash homiladorlikning rejalashtirilgan boshlanishidan kamida 2 oy oldin to’xtatilishi kerak (“Farmakokinetika” bo’limiga qarang).
Emizish davri
Emizgan kalamushlarda semaglutid sutga singib bordi. Emizgan chaqaloq uchun xavfni istisno qilib bo’lmaydi. Emizishda semaglutiddan foydalanish taqiqlanadi.
Foydalanish bo’yicha ko’rsatmalar va dozalar
Qo’llash usullari
Semavic® dori vositasi ovqatdan qat’iy nazar, haftada bir marta istalgan vaqtda qo’llaniladi. Semavic® dori vositasi teri ostiga (TO) qorin, son yoki yelkaga yuboriladi. Inyektsiya joyi dozani o’zgartirmasdan o’zgartirilishi mumkin. Semavic® dori vositasini tomir ichiga yoki mushak ichiga yuborish mumkin emas. Qo’llash usuli haqida ma’lumot “Foydalanish bo’yicha qo’llanma” bo’limida mavjud. Zarur bo’lganda, ikki inyektsiya orasidagi vaqt oralig’i kamida 3 kun (>72 soat) bo’lishi sharti bilan, haftalik qabul qilish kuni o’zgartirilishi mumkin.
Doza
Semavic® ning boshlang’ich dozasi haftada bir marta 0,25 mg ni tashkil qiladi. 4 haftalik foydalanishdan keyin dozani haftada bir marta 0,5 mg ga oshirish kerak. Glikemik nazoratni yanada yaxshilash uchun dori vositasini haftasiga bir marta 0,5 mg dozada kamida 4 hafta qo’llaganidan so’ng, dozani haftada bir marta 1 mg ga oshirish mumkin. Semavic® 0,25 mg dozasi terapevtik emas. Semavic® dori vositasi monoterapiya sifatida yoki bir yoki bir nechta gipoglikemik dorilar bilan birgalikda ishlatilishi mumkin (“Klinik samaradorlik va xavfsizlik” bo’limiga qarang). Semavic® ni metformin va/yoki tiazolidindion bilan oldingi terapiyaga qo’shganda, metformin va/yoki tiazolidindion bilan davolash xuddi shu dozalarda davom ettirilishi mumkin. Semavic® ni sulfoniluriya hosilasi yoki insulin bilan davom etayotgan terapiyaga qo’shganda, gipoglikemiya xavfini kamaytirish uchun sulfoniluriya hosilasi yoki insulin dozasini kamaytirishni hisobga olish kerak (“Maxsus ko’rsatmalar” bo’limiga qarang). Semavic®dan foydalanish qondagi glyukoza kontsentratsiyasini o’z-o’zini nazorat qilishni talab qilmaydi. Semavic® ni sulfoniluriya yoki insulin bilan birgalikda qo’llashda sulfoniluriya yoki insulin dozasini sozlash uchun qondagi glyukoza kontsentratsiyasini o’z-o’zini nazorat qilish talab qilinishi mumkin.
O’tkazib yuborilgan doza
Agar doza o’tkazib yuborilgan bo’lsa, Semavic rejalashtirilgan dozadan keyin 5 kun ichida iloji boricha tezroq kiritilishi kerak. Agar o’tkazib yuborilgan doza 5 kundan ortiq davom etsa, o’tkazib yuborilgan dozani kiritish shart emas. Semavicning keyingi dozasi muntazam ravishda belgilangan kunda kiritilishi kerak. Har holda, bemorlar odatdagi haftasiga bir marta dozalash jadvalini tiklashlari mumkin.
Bemorlarning maxsus klinik guruhlarida dori vositasini qo’llash
Bolalar va o’smirlar
Semavic®ni 18 yoshgacha bo’lgan bolalarda qo’llash samaradorlik va xavfsizlik to’g’risida ma’lumotlar yo’qligi sababli tavsiya etilmaydi.
Keksa bemorlar (≥ 65 yosh)
Yoshga qarab dozani sozlash talab qilinmaydi. 75 va undan katta yoshdagi bemorlarda semaglutid bilan ishlash tajribasi cheklangan.
Buyrak funktsiyasi buzilgan bemorlar
Buyrak yetishmovchiligi bo’lgan bemorlarda dozani sozlash talab qilinmaydi. Semavic® ni buyrak yetishmovchiligining oxirgi bosqichi bo’lgan bemorlarda qo’llash tajribasi yo’q; Bunday bemorlarda Semavic® dan foydalanish tavsiya etilmaydi.
Jigar yetishmovchiligi bo’lgan bemorlar
Jigar yetishmovchiligi bo’lgan bemorlarda dozani to’g’irlash talab qilinmaydi (“Farmakokinetika” bo’limiga qarang). Jigar etishmovchiligi bo’lgan bemorlarda semaglutidni qo’llash tajribasi cheklangan; Bunday bemorlarda Semavic® dan foydalanish tavsiya etilmaydi.
Nojo’ya ta’siri
Klinik tadqiqotlar paytida eng ko’p xabar qilingan nojo’ya ta’sirlar (NT) oshqozon-ichak kasalliklari, shu jumladan ko’ngil aynishi, ich ketish va qusish edi. Umuman olganda, bu ta’sirlar yengil va o’rtacha og’irlikda va qisqa muddatli edi. Semavic® dori vositasini qo’llashda yuzaga kelishi mumkin bo’lgan nojo’ya ta’sirlar tartibga soluvchi faoliyat uchun MedDRA lug’atiga muvofiq, ularning paydo bo’lish chastotasini ko’rsatadigan tizimli organlar sinflari bo’yicha taqsimlanadi: juda tez-tez (≥1/10), tez-tez (≥1/100, lekin <1 /10), kamdan-kam (≥1/1000, lekin <1/100), Ba’zan(≥1/10 000, lekin <1/1 000), juda kam (<1/10 000), chastotasi noma’lum (mavjud ma’lumotlarga asoslanib hisoblab bo’lmaydi). Har bir guruhda NTlarning chastotasi og’irlik darajasini pasaytirish tartibida keltirilgan.
1-jadval. 3-bosqich klinik sinovlari davomida aniqlangan salbiy ta’sirlar
| MedDRA organlari tizimi | Juda tez-tez | Tez-tez | kamdan-kam | Ba’zan |
|---|---|---|---|---|
| Immun tizimining buzilishi | Anafilaktik ta’sirlar | |||
| Metabolik va ovqatlanishning buzilishi | Insulin yoki sulfoniluriya hosilalari bilan birgalikda ishlatilganda gipoglikemiya⁽ᵃ⁾ | Boshqa og’iz gipoglikemik dori (OGGD)lar bilan birgalikda ishlatilganda gipoglikemiya⁽ᵃ⁾ Ishtahaning pasayishi | ||
| Asab tizimining buzilishlari | Bosh aylanishi | Disgeuziya | ||
| Ko’rishdagi buzilishlar | Diabetik retinopatiyaning asoratlari⁽ᵇ⁾ | |||
| Yurak kasalliklari | Yurak qisqarishi chastotasining oshishi (YuQCh) | |||
| Oshqozon-ichak trakti (OIT) sohasidagi buzilishlar | Ko’ngil aynishi, ich ketishi | Qusish, qorin og’rig’i, qorin shishi, ich qotishi, dispepsiya, gastrit, gastroezofagial reflyuks kasalligi, qichishish, meteorizm | ||
| Jigar va o’t yo’llarining buzilishi | Xolelitiyoz | |||
| Dori yuborilgan joyda umumiy buzilish hollari | Charchoq | Inyeksiya joyidagi reaktsiyalar | ||
| Laboratoriya va texnik ma’lumotlar | Lipaza faolligini oshirish, amilaza faolligini oshirish, tana vaznini kamaytirish |
⁽ᵃ⁾gipoglikemiya, og’ir (boshqa odamning yordamini talab qiladigan) yoki plazma glyukoza kontsentratsiyasi <3,1 mmol/L bilan birgalikda simptomatik tarzda aniqlanadi.
⁽ᵇ⁾Diabetik retinopatiyaning asoratlari quyidagilardan iborat: retinaning fotokoagulyatsiyasiga bo’lgan ehtiyoj, dori-darmonlarni intravitreal yuborish zarurati, shishasimon bezga qon quyilishi, diabet bilan bog’liq ko’rlikning rivojlanishi.
Chastotalik yurak-qon tomir tahlil natijalariga asoslangan
Tanlangan salbiy reaktsiyalarning tavsifi
Gipoglikemiya
Semavic® bilan monoterapiya paytida og’ir gipoglikemiya asoratlari kuzatilmadi. Semavic® dori vositasini sulfoniluriya hosilasi yoki insulin bilan birgalikda qo’llashda asosan og’ir gipoglikemiya kuzatildi. Semavic® dori vositasini boshqalar bilan birgalikda qo’llashda og’ir gipoglikemiyaning bir nechta asoratlari kuzatildi, sulfoniluriya hosilasi, OGGD bundan mustasno.
Oshqozon-ichak traktining salbiy reaktsiyalari
Semanavik® bilan 0,5 mg va 1 mg dozalarda muolaja paytida bemorlarda ko’ngil aynishi, ich ketish (diareya) va qusish kuzatildi. Aksariyat aks ta’sirlar yengil va o’rtacha og’irlikda va qisqa muddatli edi. NTlar mos ravishda 3,9% va 5,9% bemorlarda klinik tadqiqotlardan muddatidan oldin bekor qilinishiga olib keldi. Ko’p hollarda noxush ta’sirlar haqida muolajaning birinchi oylarida xabar shikoyat tushardi.
Diabetik retinopatiyaning asoratlari
2-toifa diabet va yuqori yurak-qon tomir kasalliklari, uzoq muddatli diabet va yetarli darajada glyukemik nazoratga ega bo’lmagan bemorlar ishtirok etgan 2 yillik klinik tadqiqotda diabetik retinopatiya asoratlarining tasdiqlangan holatlari platsebo (1,8 %) qabul qilgan bemorlarga nisbatan Semavic® (3,0 %) qabul qilgan bemorlarning ko’proq qismida rivojlangan. KT boshida diabetik retinopatiya tarixi bo’lgan bemorlarda asoratlarni rivojlanishining mutlaq xavfi yuqori bo’lgan. Tasdiqlangan diabetik retinopatiya tarixi bo’lmagan bemorlarda hodisalar soni Semanavik® va platsebo bilan bir xil edi. 1 yilgacha davom etgan klinik tadqiqotlarda diabetik retinopatiya bilan bog’liq nojo’ya reaktsiyalar tez-tez takrorlanishi Semavic® guruhi va taqqoslash dori vositalarida o’xshash edi.
Noxush ta’sir tufayli davolanishni to’xtatish
Semanavik® 1 mg qabul qilgan bemorlarda NT tufayli dori vositasini to’xtatish darajasi 8,7 % ni tashkil etdi. Davolashni to’xtatishga olib keladigan eng ko’p uchraydigan salbiy reaktsiyalar oshqozon-ichak kasalliklari edi.
Inyeksiya joyidagi reaktsiyalar
Semaglutidni 0,5 mg va 1 mg qabul qilgan bemorlarning mos ravishda 0,6% va 0,5% da inyeksiya joyidagi reaktsiyalar (masalan, inyeksiya joyida toshma, qizarish) qayd etilgan. Bu reaktsiyalar odatda yengil o’tar edi.
Immunogenlik
Protein va peptidli dorilarning ehtimoliy immunogen xususiyatlari tufayli bemorlar Semavic® bilan davolashdan keyin semaglutidga antikorlarni rivojlanishi mumkin. Sinov oxirida har qanday vaqtda semaglutidga antikorlari bo’lgan bemorlarning nisbati past edi (1–2 %) va hech bir bemorda semaglutidga qarshi antikorlar yoki endogen GSP-1 neytrallashtiruvchi ta’sirga ega antikorlar yo’q edi.
Agar yo’riqnomada sanab o’tilgan dori vositalarining har qanday nojo’ya ta’siri yomonlashsa yoki ko’rsatmalarda ko’rsatilmagan boshqa nojo’ya reaktsiyalar yuzaga kelsa, bu haqda shifokorga xabar berish kerak.
Dozani oshirib yuborish
Belgilar
Klinik tadqiqotlarda bitta dozada 4 mg gacha va haftasiga 4 mg gacha bo’lgan dozani oshirib yuborish holatlari qayd etilgan. Eng ko’p uchraydigan NT ko’ngil aynish edi. Barcha bemorlar asoratsiz tuzalib ketishdi.
Davolash
Semavic® dozasini oshirib yuborish uchun maxsus antidot mavjud emas. Dozani oshirib yuborish holatlarida tegishli simptomatik davolash tavsiya etiladi. dori vositasini uzoq vaqt yo’q qilish davrini (taxminan 1 hafta) hisobga olgan holda, dozani oshirib yuborish belgilari uchun uzoq muddatli kuzatuv va davolash talab qilinishi mumkin.
Boshqa dorilar bilan o’zaro ta’siri
Farmakodinamik o’zaro ta’sirlar
Semaglutid bilan olib borilgan in vitro tadqiqotlar sitoxrom P450 (CYP) fermentlarini yuborish yoki induktsiya qilish va dori tashuvchilarni yuborish uchun juda past ehtimolni ko’rsatdi. Semaglutid bilan oshqozonni bo’shatishning kechikishi bir vaqtning o’zida og’iz orqali qabul qilinadigan dorilarning so’rilishiga ta’sir qilishi mumkin.
Semaglutid oshqozon-ichak traktidan tez so’rilishini talab qiladigan og’iz orqali yuboriladigan dori vositalarini qabul qilgan bemorlarda ehtiyotkorlik bilan qo’llanilishi kerak.
Paratsetamol
Paratsetamolning farmakokinetikasini standartlashtirilgan ovqatlanish testida baholashda semaglutid oshqozon bo’shatishini kechiktirishi aniqlandi. Semaglutid 1 mg dozada birgalikda qo’llanilganda, paratsetamolning AUC0–60 min va Cmaks mos ravishda 27 % va 23 % ga kamaydi. Paratsetamolning umumiy ta’siri (AUC0–5 soat) o’zgarmadi. Semaglutid va paratsetamolni bir vaqtning o’zida qabul qilganda, ikkinchisining dozasini sozlash talab qilinmaydi.
Og’iz orqali gormonal kontratseptivlar
Semaglutidning og’iz orqali yuboriladigan gormonal kontratseptivlarning samaradorligini kamaytirishi kutilmaydi. Semaglutid bilan birlashtirilgan gormonal kontratseptiv (0,03 mg etinil estradiol / 0,15 mg levonorgestrel) qo’llanganda, ikkinchisi etinil estradiol va levonorgestrelning umumiy ta’siriga klinik jihatdan ahamiyatli ta’sir ko’rsatmadi. Etinil estradiol ta’siriga ta’sir qilmadi; Barqaror holatdagi levonorgestrel ta’sirining 20 % ga ortishi kuzatildi. Cmax hech bir komponent uchun o’zgarmadi.
Atorvastatin
Semaglutid atorvastatinning bir martalik dozasini (40 mg) qabul qilgandan keyin atorvastatinning tizimli ta’sirini o’zgartirmadi. Atorvastatinning Cmaksi 38% ga kamaydi. Ushbu o’zgarish klinik jihatdan ahamiyatsiz deb hisoblanadi.
Digoksin
Semaglutid digoksinning bir martalik dozasini (0,5 mg) qabul qilgandan so’ng digoksinning tizimli ta’sirini yoki Cmaksni o’zgartirmadi.
Metformin
Semaglutid 3,5 kun davomida kuniga ikki marta 500 mg metformin qabul qilinganidan keyin metforminning tizimli ta’sirini yoki Cmaksni o’zgartirmadi.
Varfarin
Semaglutid warfarinning bir martalik dozasini (25 mg) qabul qilgandan so’ng, varfarinning R- va S-izomerlarining tizimli ta’sirini yoki Cmaksni o’zgartirmadi. Xalqaro normallashtirilgan munosabat (XNM)ni aniqlash asosida warfarinning farmakodinamik ta’sirida klinik jihatdan ahamiyatli o’zgarishlar kuzatilmadi.
Mos kelmaslik
Semavic® dori vositasiini boshqa dorivor dori vositasilar, shu jumladan infuzion eritmalar bilan aralashtirish mumkin emas. Semavic® ga qo’shilgan moddalar semaglutidning parchalanishiga olib kelishi mumkin.
Maxsus ko’rsatmalar
Semanavik® dan foydalanish 1-toifa diabet bilan og’rigan bemorlarda yoki diabetik ketoatsidozni davolashda taqiqlanadi. Semavic® dori vositasii insulin o’rnini bosmaydi
Oshqozon-ichak (Gastrointestinal) trakti reaktsiyalar
GSP-1R agonistlarini qo’llash oshqozon-ichak traktining salbiy reaktsiyalari bilan bog’liq bo’lishi mumkin. Buyrak etishmovchiligi bo’lgan bemorlarni davolashda buni hisobga olish kerak, chunki ko’ngil aynishi, qusish va diareya suvsizlanishga va buyrak funktsiyasining yomonlashishiga olib kelishi mumkin.
O’tkir pankreatit
GSP-1R agonistlarini qo’llash bilan o’tkir pankreatit holatlari kuzatilgan. Bemorlarga o’tkir pankreatitning xarakterli belgilari haqida xabar berish kerak. Agar pankreatitga shubha bo’lsa, Semanavik® bilan davolashni to’xtatish kerak; Agar o’tkir pankreatit tasdiqlansa, Semanavik® bilan davolashni davom ettirmaslik kerak. Pankreatit tarixi bo’lgan bemorlarda ehtiyot bo’lish kerak. O’tkir pankreatitning boshqa belgilari va belgilari bo’lmasa, oshqozon osti bezi fermentlarining faolligi oshishi o’tkir pankreatitning rivojlanishi uchun prognostik omil emas.
Gipoglikemiya
Semavic® ni sulfoniluriya hosilalari yoki insulin bilan birgalikda olgan bemorlarda gipoglikemiya rivojlanish xavfi yuqori bo’lishi mumkin. Semanavik® bilan davolanishning boshida sulfoniluriya hosilasi yoki insulin dozasini kamaytirish orqali gipoglikemiya xavfini kamaytirish mumkin.
Diabetik retinopatiya
Mavjud diabetik retinopatiyasi bo’lgan insulin va semaglutid terapiyasini olgan bemorlarda diabetik retinopatiyaning asoratlari rivojlanish xavfi yuqori bo’lgan (4.8-bo’limga qarang (Nojo’ya ta’siri)). Bunday bemorlarni diqqat bilan kuzatib borish va klinik ko’rsatmalarga muvofiq davolash kerak. Bunday bemorlar klinik tavsiyalarga muvofiq doimiy kuzatuv ostida bo'lishlari va muolaja olishlari kerak. Glisemik nazoratning tez yaxshilanishi diabetik retinopatiyaning vaqtincha yomonlashishi bilan bog’liq, ammo boshqa sabablarni istisno qilib bo’lmaydi.
Yurak yetishmovchiligi
NYHA tasnifiga ko’ra, CHF funktsional klassi IV bo’lgan bemorlarda Semavic® ni qo’llash tajribasi yo’q. Bunday bemorlarda dori vositasini qo’llash kontrendikedir.
Qalqonsimon bez (buqoq) kasalliklari
Boshqa GSP-1 analogi liraglutiddan foydalanishning marketingdan keyingi davrida qalqonsimon bezning medullar saratoni (MTC) holatlari haqida xabar berilgan. Mavjud ma’lumotlar qalqonsimon bez yuqori tabaqalanuvchi saratoni (QBTS) rivojlanishi va GSP-1 analoglaridan foydalanish o’rtasidagi sababiy bog’liqlikni o’rnatish yoki istisno qilish uchun yetarli emas. Bemorga MTC xavfi va qalqonsimon bez shishi belgilari (bo’yinda shish paydo bo’lishi, disfagiya, nafas qisilishi, ovozning doimiy bo’g’ilishi) haqida ma’lumot berish kerak. Plazma kalsitonin kontsentratsiyasining sezilarli darajada oshishi QBTSni ko’rsatishi mumkin (QBTS bilan og’rigan bemorlarda plazma kalsitonin kontsentratsiyasi odatda >50 ng/L ni tashkil qiladi). Agar plazmadagi kalsitonin kontsentratsiyasining ortishi aniqlansa, bemorni qo’shimcha tekshirish kerak. Jismoniy tekshiruv yoki qalqonsimon bezning ultratovush tekshiruvi paytida aniqlangan qalqonsimon bez tugunlari bo’lgan bemorlar ham qo’shimcha tekshiruvdan o’tishlari kerak. Shaxsiy yoki oilaviy QBTS tarixi bo’lgan yoki ko’plab endokrin neoplaziya (KEN) 2-toifa sindromi bo’lgan bemorlarda semaglutidni qo’llash taqiqlanadi.
Klinikadan oldingi xavfsizlik ma’lumotlari
Xavfsizlik farmakologiyasi, takroriy dozaning toksikligi va genotoksiklikni o’rganishga asoslangan klinikadan oldingi ma’lumotlar odamlar uchun hech qanday xavfni aniqlamadi. Kalamushlar va sichqonlarda klinik ahamiyatga ega bo’lgan konsentratsiyalarda 2 yillik kanserogenlik tadqiqotlarida semaglutid o’limga olib kelmaydigan qalqonsimon C-hujayrali o’smalarini keltirib chiqardi. Sichqonlarda kuzatilgan o’limga olib kelmaydigan qalqonsimon C-hujayrali o’smalari GSP-1 analog guruhiga xosdir. Odamlar uchun xavf past deb hisoblanadi, ammo uni butunlay inkor etib bo’lmaydi.
Fertillik
Semaglutidning odamlarda fertillikka ta’siri noma’lum. Semaglutid erkak kalamushlarda unumdorlikka ta’sir qilmadi. Ayol kalamushlarda ayol tana vaznining pasayishi bilan bog’liq dozalarda estrus siklining ko’payishi va ovulyatsiya sonining biroz kamayishi kuzatildi.
Avtotransportni boshqarish va mexanizmlarni boshqarish qobiliyatiga ta’siri
Semavic® dori vositasii transport vositalarini boshqarish yoki mexanizmlar bilan ishlash qobiliyatiga ta’sir qilmaydi yoki ozgina ta’sir qiladi. Bemorlarga transport vositalarini boshqarish yoki mexanizmlar bilan ishlashda, ayniqsa Semanavik® ni sulfoniluriya hosilasi yoki insulin bilan birgalikda qo’llashda gipoglikemiya rivojlanishining oldini olish uchun ehtiyot choralarini ko’rish kerakligi haqida ogohlantirish kerak.
Foydalanuvchi uchun qo’llanma
Oldindan to’ldirilgan Semavic® shprits-dastaksi 0,25 mg, 0,5 mg va 1 mg dozalarni yuborish imkonini beradi. Bitta shprits-dastakda 3 mL eritma mavjud. Semavic® dori vositasiining o’ramida bir marta ishlatiladigan ignalar mavjud. Bemorga har bir inyektsiyadan keyin mahalliy talablarga muvofiq inyektsiya ignasini tashlab yuborish tavsiya qilinishi kerak. Semavic® shprits-dastak faqat individual foydalanish uchun mo’ljallangan. Semavic® tiniq, rangsiz yoki deyarli rangsiz eritmadan boshqa narsa ko’rinadigan bo’lsa, ishlatilmasligi kerak. Semavic® muzlatilgan bo’lsa, ishlatilmasligi kerak. Semavic®ni uzunligi 8 mm gacha bo’lgan ignalar yordamida yuborish mumkin. Shprits-dastak bir martalik inyektsiya ignalari bilan foydalanish uchun mo’ljallangan. Har bir inyektsiyadan keyin har doim ignani olib tashlang va Semavic® shprits-dastagini igna olib tashlangan holda saqlang. Bu igna tiqilib qolishi, ifloslanish, infektsiya, oqish va noto’g’ri dozalashning oldini olishga yordam beradi.
Chiqarish shakli
Teri ostiga yuborish uchun eritma, 1,34 mg/mL. 3 mL dori vositasi rangsiz neytral shisha kartridjlarda rezina pistonli, alyuminiy qopqoqli rezina diskli birlashtirilgan. Ultrium bir nechta inyektsiya uchun plastik ko’p dozali bir martalik shprits-dastakga o’rnatiladi. Har bir shprits-dastakning tanasiga polipropilen plyonkadan tayyorlangan yorliq yopishtiriladi. Ko‘p martalik inyeksiyalar uchun 1 dona oldindan to‘ldirilgan ko‘p dozali bir martali ishlatiladigan shprits-dastaklari va dori vositasini tibbiy qo‘llash bo‘yicha ko‘rsatmalar va shprits-dastakni ishlatish bo‘yicha ko‘rsatmalar bilan birga 4 ta bir martalik ignalar karton qutiga joylashtirilgan.
Yaroqlilik muddati
2 yil. shprits-dastak yorlig’i va o’ramida ko’rsatilgan yaroqlilik muddati o’tganidan keyin foydalanmang.
Saqlash shartlari
2 °C dan 8 °C gacha bo’lgan haroratda (muzlatgichda) saqlang, lekin muzlatgich yaqinida emas. Nurdan himoya qiling. Muzlatmang. Ishlatilgan yoki zaxira shprits sifatida olib yuriladigan shprits-dastakni dori vositasi bilan birga 30 °C dan yuqori bo’lmagan haroratda yoki 2 °C dan 8 °C gacha bo’lgan haroratda (muzlatgichda) 6 hafta davomida saqlang. Muzlatmang. Foydalanishdan keyin yorug’likdan himoya qilish uchun shprits-dastak qopqog’ini yoping. Semavic® haddan tashqari issiqlik va yorug’lik ta’siridan himoyalangan bo’lishi kerak. Bolalar qo’li yetmaydigan joyda saqlang.
Dam olish shartlari
Retsept bo’yicha mavjud.
Ishlab chiqaruvchi
OOO “GEROPHARM”, Rossiya Federatsiyasi
Ishlab chiqarish jarayonining barcha bosqichlari:
1. 142279, Rossiya, Moskva viloyati, Serpuxov shahar okrugi, Obolensk ishchilar posyolkasi, “A Kvartal” hududi, 5-bino, bino. 1
2. 142279, Rossiya, Moskva viloyati, Serpuxov shahar okrugi, Obolensk ishchilar posyolkasi, “A Kvartal” hududi, 4-bino, bino. 82
Iste’molchilarning da’volarini qabul qiladigan tashkilot
OOO “GEROPHARM”, Rossiya Federatsiyasi 196608, Sankt-Peterburg, Pushkin, Yachevskiy proezd, 4, 1-bino Telefon: +7 (812) 493-55-01 Faks: +7 (812) 493-55-69 Ishonch telefoni: 8-800-333-4376 (Rossiya ichida), veb-sahifa: www.geropharm.ru
Iltimos, nojo’ya reaktsiyalar haqida ma’lumotni inform@geropharm.ru elektron pochta manziliga yuboring; farmakonadzor@geropharm.com yoki OOO “GEROPHARM” ning yuqoridagi kontaktlari orqali.
UnoPen GM-B1 injektori oldindan to’ldirilgan, bir marta ishlatiladigan, ko’p martalik inyektsiya uchun mo’ljallangan shprits-dastak (keyingi o’rinlarda “Shprits-dastak” deb yuritiladi), glyukagonga o’xshash peptid-1 (GSP-1) – Semaglutidning analogi bo’lgan gipoglikemik vositani o’z ichiga oladi. Semavic® (0,25 mg/doza, 0,5 mg/doza, 1,0 mg/doza) – 0,25 mg, 0,5 mg va 1,0 mg dozalarni yuborish imkonini beruvchi oldindan to’ldirilgan shpritsli dastakda teri ostiga yuborish uchun eritma. shprits-dastak 0,25 mg dozani titrlash va 0,5 mg va 1,0 mg terapevtik dozani saqlash uchun mo’ljallangan. Bitta shprits-dastakda 3 mL eritma mavjud.
Semavic® ni qo’llashda shprits-dastakni ishlatish variantlari:
Variant 1 - dozani titrlash
0,25 mg dan 4 ta inyektsiya
0,5 mg dan 4 ta inyektsiya
1,0 mg dan 1 inyektsiya
Variant 2 - terapevtik dozani saqlash
1,0 mg dan 4 ta inyektsiya
shprits-dastak BD Micro-Fine™ Plus bir martalik inyektsiya ignalari bilan foydalanish uchun mo’ljallangan. Semavic® dori vositasiining o’ramiga 4 dona hajmdagi WellFine 4 mm 32G yoki Dexfine 4 mm 32G yoki Verifine 4 mm 32G ignalari kiradi.
Semavic®ni uzunligi 8 mm gacha bo’lgan ignalar yordamida yuborish mumkin.
Har bir inyektsiyadan oldin yangi igna qo’llanilishi kerak. inyektsiyadan keyin shprits-dastakni ignasiz saqlash va tashish kerak! Bu igna tiqilib qolishi, ifloslanishi, infektsiyasi, eritmaning oqishi va dori vositasining noto’g’ri dozasini kiritishning oldini oladi. Ignalar mahalliy talablarga muvofiq va potentsial yuqumli materiallar bilan ishlash qoidalari va qoidalariga muvofiq yo’q qilinishi kerak. shprits-dastakni ishlatish faqat bir kishi tomonidan amalga oshirilishi kerak. shprits-dastakni uchinchi shaxslarga bermaslik kerak.
Agar shprits-dastakdagi Semanavik® dori vositasii rangsiz shaffof eritmadan boshqa narsaga o’xshasa, uni ishlatmaslik kerak.
Tutqichlarni past (+2 °C dan past) yoki yuqori (+30 °C dan yuqori) haroratlarga ta’sir qilmang. shprits-dastaklarni muzlatgichga qo’ymang. shprits-dastaklarini muzlatib qo’ymang!
Ishlatilgan shprits-dastaklarni utilizatsiya qilish va qayta ishlatmaslik (qayta to’ldirish) kerak.
shprits-dastaklarini yuqori/past havo haroratida maxsus termal sumkada/sumkada (masalan, asl GEROPHARM termal qutisi) tashish yaxshiroqdir.
shprits-dastak va ignalarni boshqalarning, ayniqsa bolalarning qo’li etmaydigan joyda saqlang.
shprits-dastakni o’zingiz ta’mirlashga urinmang. Buzilgan taqdirda, dori vositasini tibbiy qo’llash bo’yicha yo’riqnomada ko’rsatilgan iste’molchi da’volarini qabul qiluvchi tashkilotga xabar bering.
GEROPHARM ma’lumot telefoni: 8 (800) 333-43-76.
Oldindan to’ldirilgan shpritsli shprits-dastak ichida teri ostiga yuborish uchun eritma (bir martalik ko’p dozali bir martalik inyektsiya uchun)
Iltimos, Semavic® shprits-dastakini ishlatishdan oldin ushbu ko’rsatmalarni diqqat bilan o’qing.
shprits-dastakni faqat shifokor yoki hamshiraning rahbarligi ostida ishlatishni o’rganganingizdan keyin foydalaning.
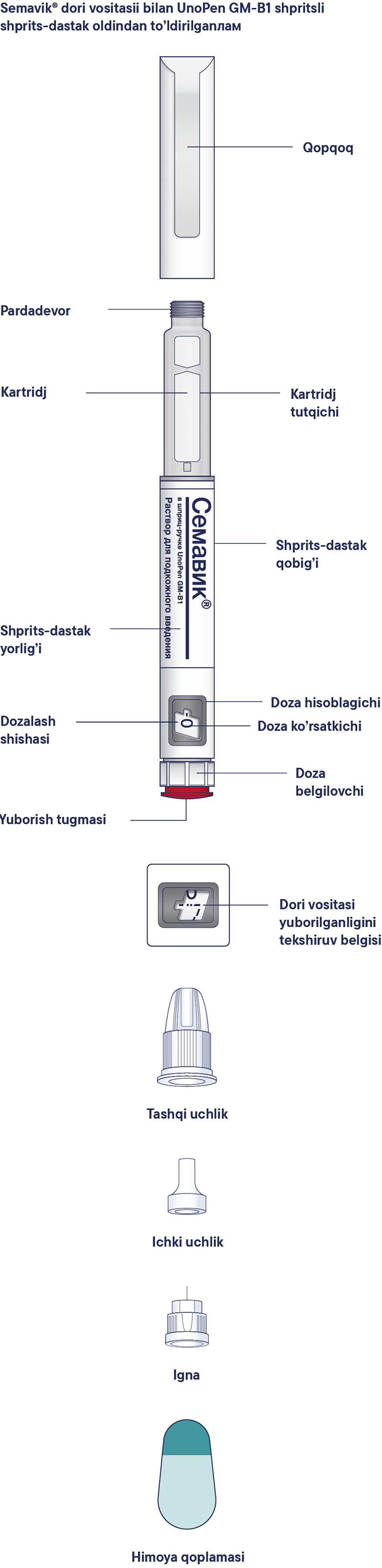
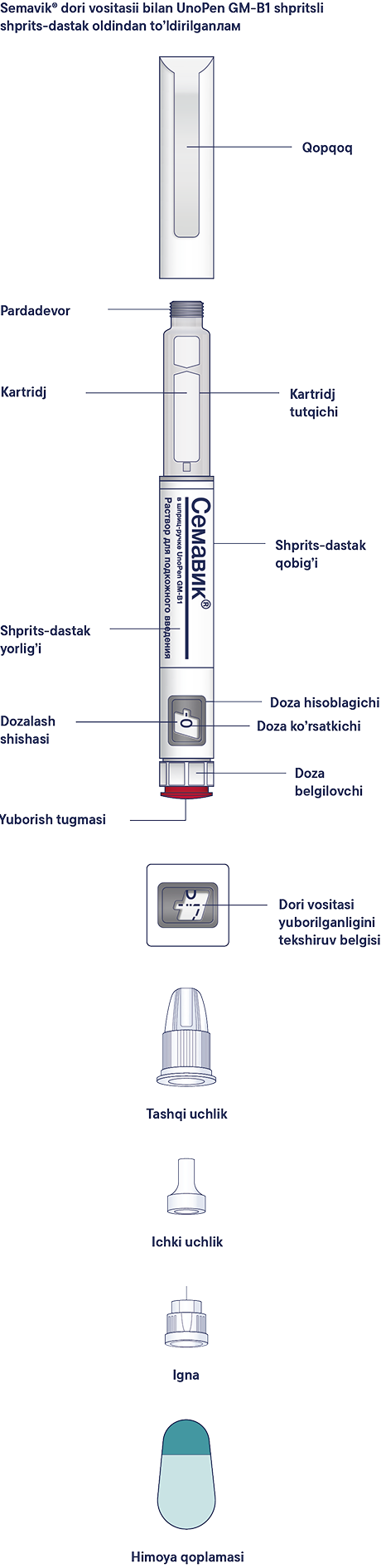
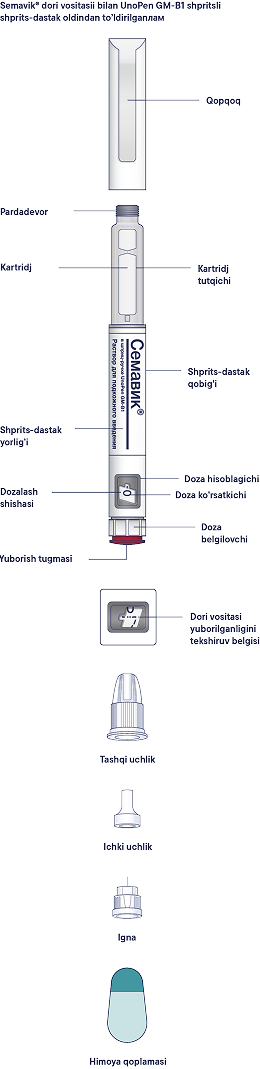
Tarkibida Semavic® 0,25 mg/doza, 0,5 mg/doza yoki 1 mg/doza borligiga ishonch hosil qilish uchun shprits-dastagingizni tekshirishdan boshlang, so’ngra shprits-dastak va ignaning turli qismlari bilan tanishish uchun quyidagi rasmlarga qarang.
Agar sizda ko‘rish qobiliyati zaif bo‘lsa yoki ko‘rishda jiddiy muammolar bo‘lsa va doza hisoblagichidagi raqamlarni ko‘ra olmasangiz, shprits-dastakni yordamisiz ishlatmang. Semavic® ni o’z ichiga olgan oldindan to’ldirilgan shprits-dastakdan foydalanishni o’rgatgan yaxshi ko’rish qobiliyatiga ega odam sizga yordam berishi mumkin.
Bu shprits-dastak oldindan to’ldirilgan shprits-dastakdir. U 4 mg semaglutidni o’z ichiga oladi va 0,25 mg, 0,5 mg yoki 1 mg dozani tanlashni taklif qiladi. shprits-dastak uzunligi 8 mm gacha bo’lgan bir martalik ignalar bilan foydalanish uchun mo’ljallangan.
Ignalilar paketga kiritilgan.
Muhim ma’lumotlar
Iltimos, bunday belgilar bilan belgilangan ma’lumotlarga alohida e’tibor bering, bu shprits-dastakni xavfsiz ishlatish uchun juda muhimdir.
Har bir inyektsiyadan keyin qulay inyektsiyani ta’minlash va ignalar tiqilib qolmasligi uchun ignani har doim tashlang. Agar igna tiqilib qolsa, siz dori vositasini AOK qila olmaysiz. Shifokoringiz, hamshirangiz, farmatsevtingiz yoki mahalliy talablar ko’rsatmasi bo’yicha olib tashlangan igna bilan bo’sh shprits-dastakngizni tashlang. Hech qachon ichki qopqoqni igna ustiga qo’yishga urinmang. Siz chayqalib qolishingiz mumkin. Har bir inyektsiyadan so’ng darhol ignani shprits-dastakdan olib tashlang. Bu igna tiqilib qolishi, ifloslanishi, infektsiyasi, eritmaning oqishi va dori vositasini noto’g’ri kiritishning oldini oladi.
Qo’shimcha muhim ma’lumotlar
shprits-dastakngizga g’amxo’rlik qilish
shprits-dastakni ehtiyotkorlik bilan tuting. Ehtiyotsiz foydalanish yoki noto’g’ri foydalanish dori vositasining noto’g’ri dozasini keltirib chiqarishi mumkin, bu esa qonda glyukoza darajasining oshishi yoki qorin bo’shlig’ida noqulaylik (ko’ngil aynishi yoki qusish) ga olib kelishi mumkin.
Birinchi inyektsiyadan oldin, oldindan to’ldirilgan bir martalik UnoPen GM-B1 shprits-dastaklarini ishlatish bo’yicha ko’rsatmalarni diqqat bilan o’qing va o’rganing.
Шприц-қаламды қолдану бойынша емдеушi дәрiгермен (маманмен) кеңесу қажет. Шприц-қаламның дұрыс қолданылуын көрсетудi сұраңыз. Препараттың алғашқы инъекциясы дәрiгердiң немесе медбикенiң бақылауымен жүргiзiлуi тиiс.
shprits-dastakchasidagi yorliqni diqqat bilan o’qing va shifokoringiz tomonidan tayinlangan aniq dori-darmonlarni, to’g’ri dozada ishlatayotganingizga ishonch hosil qiling, shuningdek, dori vositasining yaroqlilik muddatini tekshiring. Keyin shprits-dastakning xususiyatlari va qismlari bilan tanishish uchun quyidagi rasmlarga qarang.
shprits-dastakni ishlatishdan oldin uni ko’rinadigan mexanik shikastlanishlar, oqmalar (kartrij muhrining buzilishini ko’rsatuvchi) uchun tekshirish kerak. Agar shprits-dastak yaxshi holatda ekanligiga va shikastlanmaganligiga ishonchingiz komil bo’lmasa, hech qachon shprits-dastakni ishlatmang. Har bir inyektsiyadan oldin har doim shprits-dastakingizni tekshiring.
shprits-dastakni ishlatish bo’yicha ko’rsatmalarga diqqat bilan amal qiling: shprits-dastak tushishi va boshqa tashqi omillar (termik ta’sir, to’g’ridan-to’g’ri quyosh nuri, mexanik shikastlanish va boshqalar) ta’siridan saqlaning. Agar zarar bo’lsa, siz yangi shprits-dastakdan foydalanishni boshlashingiz kerak.
Ko’rish qobiliyati zaif yoki jiddiy ko’rish muammolari bo’lgan va dozani hisoblagichdagi raqamlarni ajrata olmaydigan bemor shprits-dastakni tibbiy xodim, qarindoshi yoki dori vositasini oldindan to’ldirilgan shprits-dastak bilan yuborishni o’rgangan yaxshi ko’rish qobiliyatiga ega shaxs nazorati ostida ishlatishi kerak.
Ehtiyotkorlar igna tayoqchasi shikastlanishi va o’zaro infektsiyani oldini olish uchun ishlatilgan ignalarni juda ehtiyotkorlik bilan ishlatishlari kerak.
Semavic® dori vositasii bilan UnoPen GM-B1 shpritsli shprits-dastak oldindan to’ldirilgan